Anatomie normale
La valve aortique n'est pas une structure isolée faite seulement de trois feuillets. Comme la valve mitrale, elle fait partie d'un ensemble dynamique qui constitue la voie d'éjection gauche et la racine de l’aorte. Cet ensemble comprend plusieurs éléments (Figure 26.66) [5,9].
La valve aortique n'est pas une structure isolée faite seulement de trois feuillets. Comme la valve mitrale, elle fait partie d'un ensemble dynamique qui constitue la voie d'éjection gauche et la racine de l’aorte. Cet ensemble comprend plusieurs éléments (Figure 26.66) [5,9].
- Chambre de chasse du VG (CCVG), dont les parois sont constituées par le feuillet antérieur de la valve mitrale, le septum interventriculaire et la paroi postérieure du VG. La section de la CCVG est ovale, le petit axe étant vertical et le long axe antéro-postérieur; cette forme ovale est plus prononcée à la jonction avec le ventricule car la CCVG devient progressivement plus circulaire en se rapprochant de la valve aortique [7]. La jonction entre la musculature de la CCVG et le tissu fibreux de l'aorte est abusivement décrite comme anneau aortique alors qu'il n'existe aucune structure anatomique propre à ce niveau.
- Structure aortique fibreuse en forme de couronne à 3 branches verticales remontant aux commissures des cuspides. Elle définit 3 triangles fibreux intervalvulaires dans la paroi des sinus de Valsalva, qui sont le système de sustentation des cuspides. Les valves aortique et mitrale sont contiguës: la base du feuillet mitral antérieur est insérée sur le trigone fibreux en face des feuillets aortiques gauche et non-coronaire (Figure 26.67).
- Trois cuspides de forme semi-lunaire, définies par leur corps, par leur bord libre et par leur base implantée en "U" sur la paroi aortique en regard de chaque sinus de Valsalva; la base mesure 1.5 fois le bord libre. Le point le plus bas de l'insertion des cuspides est situé sur une ligne circulaire virtuelle qui est anatomiquement dans la CCVG, en-dessous de la jonction entre l’aorte et le VG. Bien qu'elle ne coïncide avec aucune structure anatomique, cette ligne correspond à ce qu'on identifie comme l'anneau aortique en échocardiographie, car c'est le passage le plus étroit de la voie d'éjection gauche. Les commissures sont suspendues au niveau de la jonction sino-tubulaire.
- Trois sinus de Valsalva, qui sont des renflements de la racine aortique en regard des cuspides; la coronaire droite part du sinus droit (le plus antérieur); le tronc commun part du sinus gauche; le sinus non-coronaire est le plus postérieur. Leur présence évite que les cuspides ne viennent se coller à la paroi en systole et ne se referment pas assez rapidement en diastole.
- Jonction sino-tubulaire entre les sinus de Valsalva et l’aorte ascendante, au niveau de laquelle sont retenues les commissures de la valve.
- Aorte ascendante, partie tubulaire de diamètre uniforme.
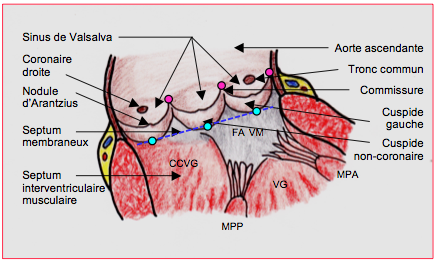
Figure 26.66 : Valve aortique ouverte in situ. Les 3 cuspides sont insérées en "U" dans la racine aortique; elles sont suspendues au niveau de la jonction sino-aortique et sont articulées comme une charnière au nadir de leur insertion (points bleus) ; ces 3 points sont situés sur l’anneau basal virtuel (traitillé bleu), qui est anatomiquement dans la chambre de chasse du VG, en-dessous de la jonction entre l’aorte et le VG. C’est l’endroit le plus rétréci de l’ensemble CCVG-racine aortique ; c’est aussi la structure que l’on mesure à l’écho comme anneau aortique, mais cette "structure" n'a pas de corrélat anatomique. Les 3 points commissuraux (points violets) sont situées sur la jonction sino-tubulaire. FAM : feuillet antérieur de la valve mitrale. MPA : muscle papillaire antérieur. MPP : muscle papillaire postérieur.

Figure 26.67: Représentation schématique de la racine aortique. Les 3 cuspides sont insérées en "U" dans la racine aortique (trait noir), au niveau des sinus de Valsalva ; elles sont suspendues au niveau de la jonction sino-tubulaire (pointillé rouge) et sont articulées par une charnière au nadir de leur insertion (points bleus) ; ces 3 points sont situés sur l’anneau basal (pointillé bleu), qui est en fait dans la chambre de chasse du VG, en-dessous de la jonction entre l’aorte et le VG (pointillé vert). Cet anneau basal, anatomiquement virtuel, est l’endroit le plus étroit du système CCVG - racine aortique - aorte ascendante ; par convention, c’est l’endroit où se mesure le diamètre de l’"anneau" aortique. Sa forme n’est pas circulaire mais légèrement elliptique. Les 3 points commissuraux (points violets) sont situées sur la jonction sino-tubulaire ; ils sont évasés de 5-10% par rapport aux points de l’anneau basal. *: triangles fibreux de la paroi des sinus de Valsalva qui sustentent les cuspides. En cartouche, représentation de la structure fibreuse qui soutient la valve aortique; elle a la forme d'une couronne à trois branches. Flèches rouges: trigones. FAM; feuillet antérieur de la valve mitrale.
L'"anneau" aortique est simplement l’endroit le plus rétréci de l’ensemble CCVG - racine aortique - aorte ascendante ; par convention, c’est aussi l’endroit où se mesure le diamètre de la base de la valve aortique. Sa forme n’est pas circulaire mais elliptique comme celle de la chambre de chasse ; le rapport entre le petit et le grand diamètre de cette ellipse est d’environ 0.7 (moyenne 26,3 mm et 23.5 mm) [8,10]. Sa taille augmente d'environ 12% pendant la systole et sa forme elliptique devient plus circulaire [3]. Ce que l’on définit comme anneau fonctionnel aortique est donc une structure virtuelle située dans la CCVG, de section ovale, correspondant au point d’insertion le plus amont des 3 cuspides aortiques en systole.
La cuspide non-coronaire (NC) est la plus postérieure ; elle est située en regard du septum interauriculaire. La cuspide coronaire droite (CD) est la plus antérieure ; la cuspide coronaire gauche (CG) surplombe la CCVG. Leur surface est légèrement asymétrique, la cuspide non-coronaire étant la plus grande : NC > CD > CG. La partie centrale des bords libres présente un renforcement fibreux (nodule d’Arantius) qui est une structure anatomique normale. Sur la face ventriculaire des cuspides, on peut trouver des dégénérescences fibreuses (excroissances de Lambl) sous forme de filaments fins et mobiles flottant dans le flux sanguin; elles sont présentes dans 0.9% de la population mais sont peu emboligènes (voir Figure 25.153) [6].
| Anatomie de la valve aortique |
| Ensemble fonctionnel de la voie d'éjection gauche: - Chambre de chasse gauche (section ovale) - 3 cuspides semi-lunaires - Structure fibreuse en couronne à 3 triangles de sustentation verticaux - Jonction sino-tubulaire (point d'attache de la commissure des cuspides) - "Anneau" aortique virtuel: nadir d'insertion des cuspides, passage le plus étroit |
Insuffisance de la valve aortique
L’insuffisance aortique (IA) est une pathologie fréquente lorsqu’elle est mineure ; elle est présente chez 1% de la population jeune et jusqu'à 13% des personnes âgées (prévalence moyenne 5-8%) [4]. Même si elle n’a pas de signification clinique, elle peut causer une dilatation aiguë du VG lorsque celui-ci cesse de battre au moment de la cardioplégie en début de CEC (Vidéo). Elle est donc à rechercher systématiquement avant toute intervention en CEC. L’IA modérée à sévère, plus rare (prévalence 0.5%), relève anatomiquement de deux structures et de deux mécanismes différents (Figure 26.68) [1].
Vidéo: même si elle est petite, une insuffisance aortique laisse fuir la cardioplégie dans le VG dès que celui-ci cesse d'éjecter en début de CEC; le ventricule peut alors se dilater dangereusement. Le contraste spontané indique une stase dans les cavités gauches.
- Dilatation de l’anneau et de la racine aortique; les cuspides sont normales;
- Lésions de la valve proprement dite; la pathologie est située au niveau des cuspides.

Figure 26.68 : Les différents types anatomo-pathologiques d’insuffisance aortique. A : maladie annulo-ectasiante ; la racine de l’aorte ascendante et l’anneau valvulaire sont dilatés (flèches rouges), mais les cuspides sont normales (IA type I) ; le jet de l’IA est central. B : la racine de l’aorte est normale mais les cuspides sont lésées ; elles peuvent être prolabantes (IA type II) ou rétractées (IA type III). Le jet de l’IA est en général excentrique ; il est dirigé à l’opposé de la cuspide prolabante ou du côté de la cuspide rétractée.
Dans le premier cas, il s’agit de la maladie annulo-ectasiante de l’aorte ascendante: la dilatation de l’anneau et de la jonction sino-tubulaire tend les bords libres des cuspides, qui sont normales, et les empèche de coapter proprement [2]. Cette affection relève de la médianécrose cystique de l’aorte, isolée ou associée au syndrome de Marfan, de la dégénérescence dilatative de l’aorte liée à l’âge (anévrysme), ou de syndromes inflammatoires systémiques (spondylite ankylosante, syndrome de Reiter ou de Behçet, aortite syphilitique, etc). Enfin, le flap intimal d’une dissection aortique de type A peut déstabiliser l’appareil valvulaire ou prolaber à travers la valve en diastole (Vidéo).
Vidéo: vue long-axe de la racine aortique dans une dissection A; la membrane (flap) prolabe à travers la valve aortique en diastole et cause une insuffisance aortique.
Dans le deuxième cas, l’insuffisance est due à des lésions des cuspides, qui relèvent de plusieurs étiologies différentes.
- Lésion dégénérative : dégénérescence myxoïde ou fibro-élastique (prolapsus), calcifications (les blocs calciques rigides dont les valvules sont infiltrées ne permettent plus l’étanchéité en diastole) (Vidéo).
- Bicuspidie: bien que cette malformation conduise le plus souvent à une sténose, il arrive qu’elle se manifeste par une insuffisance isolée ou prédominante. La prévalence de la bicuspidie est de 1-2% dans la population générale (Vidéo) (voir Bicuspidie).
- RAA: la fusion commissurale et la rétraction cicatricielle des cuspides infiltrées de tissu fibreux les empèchent de coapter en diastole (Vidéo).
- Endocardite: la destruction des feuillets, leur perforation, ou le prolapsus de végétations à travers la valve, causent une fuite transvalvulaire; dans le pannus infectieux qui ceint la racine des cuspides peut se former un abcès, le plus fréquemment à l’angle mitro-aortique (Vidéos).
- Dilatation de la racine aortique, anévrysme.
- Perte du support commissural : traumatisme, dissection A, CIV supracristale.
- Maladie systémique: Marfan, syphilis, Ehlers-Danlos, arthrite rhumatoïde (Vidéo).
- Toxicité médicamenteuse : méthysergide, ergotamine, pergolide, fenfluramine, phentermine, aminorex, benfluorex (Mediator®) ; la toxicité des anorexiants est connue depuis le début des années ‘90. Les cuspides sont épaissies; la restriction au mouvement diastolique laisse un orifice de régurgitation triangulaire au milieu de la valve.
- A partir de 50 ans, une sclérose des cuspides et une perte de souplesse dans la racine aortique peuvent entraîner une IA triviale sans signification hémodynamique, mais tout de même à risque de dilatation du VG lors de la cardioplégie en début de CEC.
Vidéo: vues simultanées orthogonales en court-axe et en long-axe (X-Plane) d'une insuffisance aortique centrale sur lésion dégénérative.
Vidéo: reconstruction 3D d'une insuffisance aortique dans un cas de bicuspidie.
Vidéo: vue long-axe d'une insuffisance aortique de type restrictif; les cuspides remaniées et rétractées ne coaptent pas en diastole.
Vidéo: longue végétation dans un cas d'endocardite aortique entraînant une insuffisance, car les cuspides ne coaptent pas en diastole.
Vidéo: abcès mitro-aortique endocarditique causant une insuffisance de la valve aortique.
Vidéo: insuffisance aortique sur dilatation de la racine aortique dans un syndrome de Marfan: les cuspides ne peuvent pas se rejoindre en diastole.
| Insuffisance aortique |
| L'insuffisance aortique est due à deux mécanismes: - Perte du support de la racine aortique (dilatation, dissection) - Affection propre des cuspides (prolapsus, RAA, endocardite) |
© CHASSOT PG, BETTEX D. Octobre 2011, Juin 2019; dernière mise à jour, Mars 2020
Références
- BOODHWANI MJ, DE KERCHOVE L, GLINEUR D, et al. Repair-oriented classification of aortic insufficiency: impact on surgical techniques and clinical outcomes. Thorac Cardiovasc Surg 2009; 137:286-94
- DARE AJ, VEINOT JP, EDWARDS WD, et al. New observations on the etiology of aortic valve disease. Hum Pathol 1993; 24:1330
- HAMDAN A, GUETTA V, KONEN E, et al. Deformation dynamics and mechanical properties of the aortic annulus by 4-dimensional computed tomography: insights into the functional anatomy of the aortic valve complex and implications for transcatheter aortic valve therapy. J Am Coll Cardiol 2012; 59:119-27
- HYATSVILLE M. Monthly vital statistics reports. National Center for Health Statistics. Report of final mortality statistics 1999; 47(19)
- KASEL AM, CASSESE S, BLEIZIFFER S, et al. Standardized imaging for cardiac annular sizing: implications for transcatheter valve selection. JACC Cardiovasc Imaging 2013; 6:249-62
- LEITMAN M, TYOMKIN V, PELEG E, et al. Clinical significance and prevalence of valvular strands during routine echo examinations. Eur Heart J Cardiovasc Imaging 2014; 15:1226-30
- MONTEALEGRE-GALLAGOS M, MRYK R, KHABBAZ KR et al. Heterogeneity in the structure of the left ventricular outflow tract: a 3-dimensional transesophageal echocardiographic study. Anesth Analg 2016; 123:290-6
- PATEL PA, GUTSCHE JT, VERNICK WJ, et al. The functional aortic annulus in the 3D era: focus on transcatheter aortic valve replacement for the perioperative echocardiographer. J Cardiothorac Vasc Anesth 2015; 29:240-5
- ROBERTS JD, DHAWAN R, CHANEY MA, LANG RM. Aortic valve anatomy and assessment by transesophageal echocardiography. Anesth Analg 2013; 117:1286-90
- ZAMORANO JL, BADANO LP, BRUCE C, et al. EAE/ASE recommendations for the use of echocardiography in new transcatheter interventions for valvular heart disease. Eur J Echocardiogr 2011; 12:557-84
