Si une discordance auriculo-ventriculaire se rajoute à la discordance ventriculo-artérielle, la survie devient possible, car les circulations systémique et pulmonaire sont de nouveau en continuité. C'est le cas de la transposition naturellement corrigée des gros vaisseaux, ou L-TGV. Dans cette anomalie, l'AP et l'aorte sont transposées comme dans la TGV, mais les ventricules sont également inversés. De ce fait, le sang suit une séquence physiologique à travers des cavités croisées: OD → VG → AP → poumons → OG → VD → Ao (Vidéo et Figures 15.57 et 15.58).
Vidéo: Transposition naturellement corrigée des gros vaisseaux. La TGV (non visible dans cette vue) est accompagnée d'une transposition des ventricules: le VG est à droite et le VD à gauche, comme le prouvent la présence dans le VD d'un pilier septal et d'une insertion de la valve tricsupide plus apicale que celle de la mitrale.
Vidéo: Transposition naturellement corrigée des gros vaisseaux. La TGV (non visible dans cette vue) est accompagnée d'une transposition des ventricules: le VG est à droite et le VD à gauche, comme le prouvent la présence dans le VD d'un pilier septal et d'une insertion de la valve tricsupide plus apicale que celle de la mitrale.
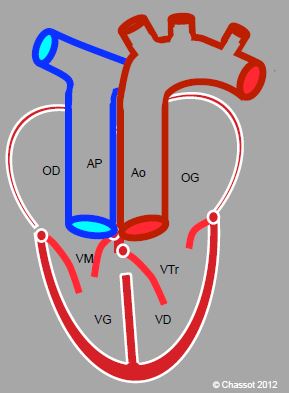
Figure 15.57 : Transposition des gros vaisseaux naturellement corrigée (L-TGV). A la discordance ventriculo-artérielle (TGV) s’ajoute une discordance auriculo-ventriculaire. L’OD est connectée à une valve mitrale (VM) et à un ventricule anatomiquement gauche (VG), puis à l’AP. Le sang oxygéné revient à l’OG par les veines pulmonaires ; l’OG se draine à travers une valve tricuspide dans un ventricule anatomiquement droit, connecté à l’aorte. Le malade n’est pas cyanosé, mais son ventricule systémique est un ventricule droit, qui défaille après 20-30 ans.


Figure 15.58 : TGV naturellement corrigée. La VCI se draine dans l’OD (situs solitus) connectée au VG, lui-même connecté à l’AP ; l’OG est connectée au VD, que l’on reconnaît à la bas-insertion de la tricuspide (flèche) ; le VD est en position sous-aortique. Le VD est hypertrophié, mais sa haute postcharge (pression systémique) a induit une insuffisance tricuspidienne massive (IT).
Le système coronarien est inversé, la CD se trouvant à gauche et le tronc commun à droite. La plupart des patients présentent une CIV périmembraneuse et des anomalies des valves auriculo-ventriculaires, notamment de type Ebstein [1,11].
Ces malades ne sont pas cyanosés, mais le ventricule anatomiquement droit se retrouve en position sous-aortique. Lorsqu’il fonctionne ainsi comme ventricule systémique, le VD s’adapte à une postcharge élevée et ressemble de plus en plus au VG: la contraction circulaire devient plus importante que la contraction longitudinale, contrairement au VD normal [8]. Mais après une vingtaine d’années à ce régime, il se dilate, développe une insuffisance tricuspidienne sévère, et devient insuffisant entre 25-40 ans; le septum interventriculaire bombe alors dans le VG et les blocs AV sont fréquents [4]. C'est souvent à ce moment-là que le diagnostic est posé. La mortalité est de 16% à 40 ans [5]. Chez l’adulte, le traitement chirurgical est centré sur l’insuffisance tricuspidienne (plastie ou remplacement), qui doit être opérée avant que la fonction du VD ne se détériore, et sur la fermeture de la CIV [2,3,9,10]. Une correction anatomique est possible dans la plupart des cas si le diagnostic est posé assez tôt, mais elle demande une préparation du VG à assumer la pression systémique par un banding préalable de l'AP pour augmenter sa postcharge et rétablir la position du septum interventriculaire; une retransposition de l'aorte et de l'AP (éventuellement avec un conduit) est réalisée ensuite [6]. La survie à long terme (10-20 ans) est de 75-85% [7]. La seule thérapeutique définitive est une transplantation, car les résultats du traitement médical chronique de l'insuffisance droite sont décevants chez les congénitaux.
Comme il assure la perfusion systémique, le VD doit bénéficier d’un soutien inotrope et d’une perfusion coronarienne optimale. Les contraintes de l’anesthésie sont dominées par l'insuffisance systolique du VD systémique, par le risque ischémique du VD et par les arythmies. Les RAS doivent être maintenues assez hautes pour assurer la perfusion coronarienne, mais sans être excessives et augmenter la postcharge du VD déjà défaillant. Le PiCCO™ est très utile pour la surveillance hémodynamique. L'ETO est essentielle pour l'évaluation de la fonction ventriculaire et de la volémie.
| Transposition des gros vaisseaux naturellement corrigée |
| A la discordance ventriculo-artérielle de la TGV s'ajoute une inversion des ventricules. Le sang suit une séquence physiologique à travers des cavités croisées: OD → VG → AP → poumons → OG → VD → Ao. Le VD est le ventricule systémique, ce qui limite la survie par défaillance droite et insuffisance tricuspidienne progressives. |
© BETTEX D, CHASSOT PG, Janvier 2008, dernière mise à jour Décembre 2019
Références
- ANDERSON R, HO SH: Echocardiographic diagnosis and description of congenital heart disease: Anatomic principles and philosophy. In ST JOHN SUTTON MG (ed): Textbook of echocardiography and Doppler in adults and children. Cambridge (MA): Blackwell Science, 1996, 711-743
- BAUMGARTNER H, BONHOEFFER P, DE GROOT NMS, et al. ESC Guidelines for the management of grown-up congenital heart disease (new version 2010). Eur Heart J 2010; 31:2915-57
- BHATT AB, FOSTER E, KUEHL K, et al. Congenital hesart disease in older adult. A Scientific Statement from the American Heart Association. Circulation 2015; 131:1884-931
- CONNELLY MS, ROBERTSON P, LIU P, et al. Congenitally corrected transposition of the great arteries in adults: Natural history. Circulation 1994; 90:I-51
- DOBSON R, DANTON M, NICOLA W, et al. The natural and un-natural history of the systemic right ventricle in adult survivors. J Thorac Cardiovasc Surg 2013; 145:1493-501
- FILIPPOV AA, DEL NIDO PJ, VASILYEV NV. Management of systemic right ventricular failure in patients with congenitally corrected transposition of the great arteries. Circulation 2016; 134:1293-302
- HIRAMATSU T, MATSUMURA G, KONUMA T, et al. Long-term prognosis of double-switch operation for congenitally corrected transposition of the great arteries. Eur J Cardiothorac Surg 2012; 42:1004-8
- PETTERSEN E, HELLE-VALLE T, EDVARDSEN T, et al. Contraction pattern of the systemic right ventricle. J Am Coll cardiol 2007; 49:2450-6
- SILVERSIDES CK, SALEHIAN O, OECHSLIN E, et al. Canadian Cardiovascular Society 2009 Consensus Conference on the management of adults with congenital heart disease: Complex congenital cardiac lesions. Can J Cardiol 2010; 26:e98-e117
- STOUT KK, DANIELS CJ, VALENTE AM, et al. 2018 AHA/ACC Guideline for the management of adults with congenital heart disease. J Am Coll Cardiol 2019; 73:e81-192
- WARNES CA, WILLIAMS RG, BASHORE TM, et al. ACC/AHA 2008 Guidelines for the management of adults with congenital heart disease: executive summary. Circulation 2008; 118:2395-451
