Comme pour l'insuffisance mitrale, la tendance chirurgicale actuelle est de procéder autant que possible à une plastie de la valve aortique au lieu d'un remplacement d'emblée par une prothèse, ce qui élimine les risques de l'anticoagulation liée aux valves mécaniques et le problème de la dégénérescence liée aux bioprothèses. Néanmoins, la plastie aortique est plus délicate que la plastie mitrale et pas encore aussi largement pratiquée. L'ETO peropératoire prend donc une place cruciale pour décider de la faisabilité d'une reconstruction et pour juger de la qualité de la réparation après la CEC. L'examen pré-CEC modifie le plan chirurgical dans 11-25% des patients et justifie une réopération dans 4-6% des cas [13].
Un bref rappel de l'anatomie est utile avant d'aborder les images échocardiographiques (Figure 11.131).
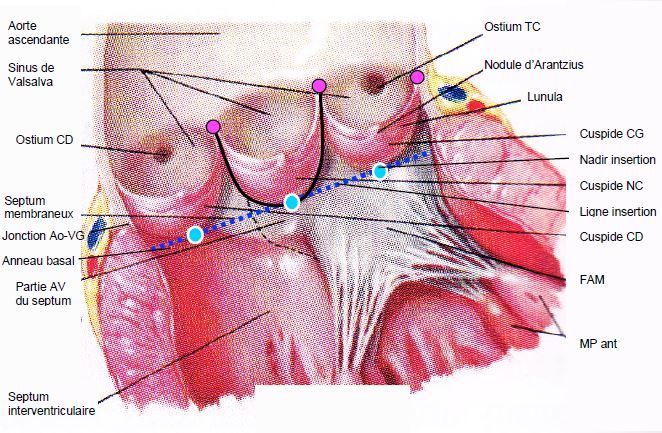
Figure 11.131 : Valve aortique ouverte in situ. Les 3 cuspides sont insérées en "U" dans la racine aortique (trait noir) ; elles sont suspendues au niveau de la jonction sino-aortique et sont articulées par une charnière au nadir de leur insertion (points bleus) ; ces 3 points sont situés sur l’anneau basal (traitillé bleu), qui est anatomiquement dans la chambre de chasse du VG, en-dessous de la jonction entre l’aorte et le VG. C’est l’endroit le plus rétréci de l’ensemble CCVG-racine aortique ; c’est aussi la structure que l’on mesure à l’écho comme anneau aortique, mais cette "structure" n'a pas de corrélat anatomique. Les 3 points commissuraux (points violets) sont situées sur la jonction sino-tubulaire. AV : atrio-ventriculaire. CD : coronaire droite. CG_ coronaire gauche. FAM : feuillet antérieur de la valve mitrale. MP : muscle papillaire. NC : non-coronaire. TC : tronc commun.
- Les 3 cuspides de la valve aortique sont suspendues au niveau de la jonction sino-aortique par les 3 points commissaux; leur insertion basse est située sur l’anneau basal virtuel, qui est anatomiquement dans la chambre de chasse du VG (CCVG), en-dessous de la jonction entre l’aorte et le VG. Leur longueur est légèrement inférieure à la distance antre l’anneau aortique et les ostia coronariens.
- Leur insertion en "U" défini 3 triangles fibreux intervalvulaires dans la paroi des sinus de Valsalva, qui forment une couronne de sustentation pour les cuspides (Figure 11.132).

Figure 11.132: Représentation schématique de la racine aortique. Les 3 cuspides sont insérées en "U" dans la racine aortique (trait noir), au niveau des sinus de Valsalva ; elles sont suspendues au niveau de la jonction sino-tubulaire (pointillé rouge) et sont articulées par une charnière au nadir de leur insertion (points bleus) ; ces 3 points sont situés sur l’anneau basal (pointillé bleu), qui est en fait dans la chambre de chasse du VG, en-dessous de la jonction entre l’aorte et le VG (pointillé vert). Cet anneau basal, anatomiquement virtuel, est l’endroit le plus étroit du système CCVG - racine aortique - aorte ascendante ; par convention, c’est l’endroit où se mesure le diamètre de l’"anneau" aortique. Sa forme n’est pas circulaire mais elliptique. Les 3 points commissuraux (points violets) sont situées sur la jonction sino-tubulaire ; ils sont évasés de 5-10% par rapport aux points de l’anneau basal. *: triangles fibreux de la paroi des sinus de Valsalva qui sustentent les cuspides.
- L'"anneau" aortique est simplement l’endroit le plus rétréci de l’ensemble CCVG - racine aortique - aorte ascendante ; par convention, c’est aussi l’endroit où se mesure le diamètre de la base de la valve aortique. Sa forme n’est pas circulaire mais elliptique comme celle de la chambre de chasse ; le rapport entre le petit et le grand diamètre de cette ellipse est d’environ 0.7 (moyenne 26,3 mm et 23.5 mm) [17,24]. Ce que l’on définit comme anneau fonctionnel aortique est donc une structure virtuelle située dans la CCVG, de section ovale, correspondant au point d’insertion le plus amont des 3 cuspides aortiques en systole. Le plan ETO long-axe à 120-140°, où l’on mesure le diamètre de l’anneau aortique, coupe l’ovale de cet anneau dans son plus petit diameter (Figures 11.133 et 11.134). L’ETO bidimensionnelle sous-estime donc le diamètre réel de l’anneau aortique, et ceci pour deux raisons [16,17]:
- La vue mi-oesophagienne long-axe (120-140°) coupe l’anneau elliptique dans son petit diamètre (plan sagittal);
- Le plan de coupe ne passe pas par le centre de l’anneau mais un peu en avant de celui-ci.
- Les sinus de Valsalva sont des renflements de l'aorte ascendant au niveau de chaque cuspide; leur présence évite que celles-ci ne viennent se coller à la paroi en systole et ne se referment pas assez rapidement en diastole.
- La jonction sino-tubulaire est l'endroit où débute l'aorte ascendante, qui a une forme de tube régulier et de section circulaire.

Figure 11.133 : Corrélation anatomo-échocardiographique des 2 plans de coupe de la valve aortique : vues ETO rétrocardiaques mi-oesophagiennes en court-axe à 40° (A) et en long axe à 120-140° (coupe sagittale) (B). Pour chacune des 2 vues sont illustrés verticalement le schéma de l’aorte, le schéma de la vue ETO et l’image ETO bidimensionnelle. L’anneau aortique est elliptique, alors que l’aorte ascendante est circulaire. Le diamètre antéro-postérieur (Ø AP) est plus court que le diamètre gauche-droit ou diamètre coronal (Ø Cor). Sur l’image en court-axe (à gauche), le traitillé blanc représente l’intersection avec le plan à 120-140° ; sur l’image en long-axe (à droite), il représente l’intersection avec le plan à 40°. Le traitillé bleu est l’intersection avec le troisième plan, qui est un plan long-axe perpendiculaire à celui de l’ETO mais qui est situé en avant du capteur oesophagien (plan gauche-droit, coronal ou frontal) et qui n’intercepte pas ce dernier ; il n’est donc visible qu’en ETO tridimensionnelle.
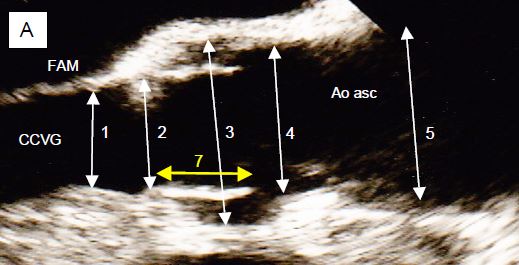

Figure 11.134 : Evaluation ETO préopératoire des diamètres aortiques. A : diamètres en long axe 120°. 1 : chambre de chasse du VG ; 2 : anneau aortique (mesure sur le bord interne, trailing edge-to-leading edge) ; 3 : sinus de Valsalva ; 4 : jonction sino-tubulaire ; 5 : aorte ascendante (au croisement de l’artère pulmonaire droite) ; 7 : hauteur de la cuspide. Ces diamètres se mesurent en systole. FAM : feuillet antérieur de la valve mitrale ; CCVG : chambre de chasse du VG. B : représentation schématique des mêmes diamètres. 6 : distance entre l’anneau aortique et l’ostium coronarien droit ; 7 : hauteur de la cuspide droite (jaune) ; normalement, 6 est > 7. C : le diamètre de l’anneau aortique (en bleu) tel qu’on le mesure en vue long-axe 120° projeté sur la vue court-axe; il est légèrement plus étroit que le diamètre anatomique réel (en pointillé), parce qu’il ne passe pas réellement par le centre de l’anneau, mais un peu antérieurement à celui-ci.
Le plan qui intercepte le plus grand diamètre de l’anneau est un plan long-axe dit coronal ou gauche-droit, perpendiculaire au plan long-axe à 120°, coupant celui-ci selon le traitillé bleu dans la Figure 11.133. Ce plan frontal est irréalisable en ETO car il est situé en avant de l’œsophage et ne passe pas par le capteur de la sonde. Seule la reconstruction tri-dimensionnelle (ETO 3D) permet de le visualiser. La vue transgastrique profonde à 0° donne une vision voisine de ce troisième plan, mais ne lui est pas exactement co-planaire ; d’autre part, cette vue donne des images distantes et imprécises de la valve aortique. Elle n’est donc pas un substitut à la reconstruction 3D. La distance entre l’anneau et l’ostium coronarien droit est bien visible dans le plan 2D long-axe 120-140° (Figure 11.134), mais celle qui sépare l’anneau de l’ostium gauche (tronc commun) n’est pas accessible à l’ETO 2D, car elle se trouve précisément dans le plan coronal gauche-droit que l’on n’obtient qu’à l’écho 3D. La valeur moyenne de la distance entre l’anneau aortique et chaque ostium est de 13.5 mm [14].
Echocardiographie bidimensionnelle
Une insuffisance aortique mineure asymptomatique est présente chez 1% de la population jeune, 5% des adultes et jusqu’à 13% des personnes âgées [7]. Même si elle n’a pas de signification clinique, elle peut causer une dilatation aiguë du VG lorsque celui-ci ralentit puis cesse de battre au moment de la cardioplégie et du clampage aortique en début de CEC (Vidéo). Elle est donc à rechercher systématiquement avant toute intervention en CEC.
Vidéo: Fuite intraventriculaire de la cardioplégie en cas d'insuffisance aortique, même mineure, lorsque le VG s'arrête et n'éjecte plus; ce flux conduit à une dilatation dangereuse du ventricule.
Par analogie à la classification des IM, on décrit 3 types d’IA, le premier type étant subdivisé en 4 catégories (voir Figure 11.127) [2,4.19].
- Type I : cuspides normales, dilatation de la racine aortique; jet d'IA central.
- Ia: dilatation de la jonction sino-tubulaire et de l'aorte ascendante;
- Ib: dilatation des sinus de Valsalva (racine aortique);
- Ic: dilatation de l'anneau aortique;
- Id: perforation d'une cuspide.
- Type II : excès de tissu et de mouvement d’une ou des cuspides, prolapsus; jet excentrique.
- Type III : mouvement restrictif des cuspides, fibrose, fusion commissurale, calcifications; jet variable.

Figure 11.127 : Les différents types anatomo-pathologiques d’insuffisance aortique selon El Khoury [7,4,19].
L'examen de la valve s'accompagne de celui de la racine aortique et de ses dimensions (vue long-axe 120° et reconstruction 3D), qui permet de décrire trois phénotypes différents dans le type I (mesures prises en télédiastole sauf pour l'anneau aortique qui est mesuré en méso-systole) [1,19].
- Dilatation de l'anneau aortique; diamètre normal: 2.1-2.3 cm chez la femme, 2.3-2.6 cm chez l'homme;
- Anévrysme de la racine aortique: diamètre au niveau des sinus de Valsalva > 4.5 cm;
- Anévrysme de l'aorte ascendante: diamètre > 5.0 cm.
La surcharge de volume au régime de pression diastolique de l’aorte entraîne une très forte dilatation du VG (diamètre télésystolique > 5.0 cm, diamètre télédiastolique > 7.0 cm, Vts > 50 mL/m2, Vtd > 135 mL/m2). L’image 2D de l’IA est caractéristique (Figure 11.135).
- Hypertrophie dilatative et sphéricisation du VG, dilatation modérée de l’OG (Vidéo).
Vidéo: Hypertrophie dilatative du VG dans un cas d'insuffisance aortique.
- Dilatation de la racine de l’aorte (IA type I) (Vidéo).
Vidéo: dilatation de la racine aortique entraînant une non-coaptation diastolique des cuspides dans un syndrome de Marfan (vues simultanées en long-axe et en court-axe).
- Prolapsus ou déchirure d’une cuspide qui bombe dans la CCVG en diastole (IA type II) (Vidéos).
Vidéo: Prolapsus de la cuspide antérieure dans une bicuspidie aortique en vue long-axe 120°.
Vidéo: Flux couleur illustrant la régurgitation diastolique dans le même cas que dans la vidéo précédente.
- Rétraction des cuspides avec orifice de régurgitation en diastole (IA type III) (Vidéo).
Vidéo: Non-occlusion de la valve aortique en diastole suite à une rétraction des cuspides, en vue long-axe 120°.
- Bombement diastolique du corps du feuillet antérieur de la valve mitrale dans l’OG ; lésion de jet (jet lesion) au point d’impact de l’IA sur ce feuillet antérieur.
- Vibration diastolique du feuillet antérieur de la valve mitrale due au jet de l’IA qui le lèche à vélocité élevée (origine du roulement de Flint) (Vidéos).
Vidéo: Roulement de Flint; si elle est dirigée vers l'extrémité du feuillet mitral antérieur, l'insuffisance aortique le fait vibrer en diastole.
Vidéo: flux Doppler couleur montrant le mécanisme de la vibration diastolique du feuillet mitral antérieur à l'origine du roulement de Flint (vue long-axe 140°).
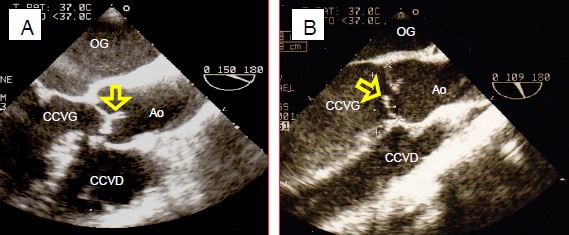
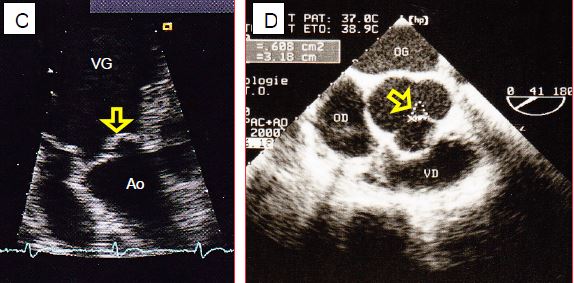
Figure 11.135 : Images bidimensionnelles d’insuffisance aortique. A : hauteur normale de coaptation des cuspides aortiques. B : prolapsus de la cuspide coronarienne droite. C : prolapsus de la cuspide non-coronaire en vue transgastrique. D : orifice de régurgitation central lors de dilatation de l’anneau ; la surface de l’orifice (0.6 cm2) signe une IA sévère.
Echocardiographie Doppler
L’image la plus caractéristique de l’IA est la présence d’un jet diastolique tourbillonnaire dans la CCVG, dont l’extension en direction du VG est une manière qualitative rapide d’évaluer l’importance de la régurgitation (Vidéos) [18].
Vidéo: Insuffisance aortique modérée en vue long-axe 130° de la racine aortique.
Vidéo: Vue court-axe 50° de l'orifice de régurgitation centrale triangulaire mis en évidence par le flux couleur persistant en diastole.
Mais cette méthode est peu performante parce qu’elle est tributaire de l’hémodynamique, des réglages de l’appareil et de l’angle d’analyse. L’extension du jet dépend de sa Vmax, qui est fonction du ΔP entre l’aorte et le VG en diastole ; elle augmente ou diminue parallèlement à la pression diastolique aortique ; elle varie également avec la compliance de l’aorte et du VG [3]. L'évaluation du jet couleur diastolique doit comprendre la partie amont (PISA), le passage à travers la valve (vena contracta) et le jet dans la CCVG et le VG. La morphologie du jet est une source de renseignements considérable (Figure 11.136 et Figure 11.137) [9].
Vidéo: Insuffisance aortique modérée en vue long-axe 130° de la racine aortique.
Vidéo: Vue court-axe 50° de l'orifice de régurgitation centrale triangulaire mis en évidence par le flux couleur persistant en diastole.
Mais cette méthode est peu performante parce qu’elle est tributaire de l’hémodynamique, des réglages de l’appareil et de l’angle d’analyse. L’extension du jet dépend de sa Vmax, qui est fonction du ΔP entre l’aorte et le VG en diastole ; elle augmente ou diminue parallèlement à la pression diastolique aortique ; elle varie également avec la compliance de l’aorte et du VG [3]. L'évaluation du jet couleur diastolique doit comprendre la partie amont (PISA), le passage à travers la valve (vena contracta) et le jet dans la CCVG et le VG. La morphologie du jet est une source de renseignements considérable (Figure 11.136 et Figure 11.137) [9].


Figure 11.136 : Insuffisance aortique. A : jet d’IA central en cas de dilatation de l’anneau (maladie de la racine de l’aorte). B : jet excentrique an cas de lésion d’une cuspide aortique (prolapsus). C : mesure du diamètre de la vena contracta juste en aval de la valve. D : rapport du diamètre du jet à celui de la chambre de chasse au même niveau.


Figure 11.137 : Flux Doppler couleur dans une IA. A : IA centrale en vue long-axe de l’aorte ascendante. B : IA centrale en vue transgastrique profonde. C : IA excentrique en vue long axe mi-oesophage. D : IA en vue court-axe.
- Un jet central de symétrie circulaire traduit une fuite liée à une dilatation de l’anneau sans lésion des cuspides (Vidéo).
Vidéo: Insuffisance aortique centrale sur dilatation de la racine aortique dans un syndrome de Marfan (vue long-axe 160°).
- Un jet excentrique est dû à une lésion de la valve elle-même ; la fuite est dirigée à l’opposé de la cuspide qui prolabe ou du côté de celle qui est rétractée (Vidéo).
Vidéo: Insuffisance aortique excentrique due à un prolapsus de la cuspide coronarienne droite (vue long-axe 130°).
- Le flux couleur comprend 3 zones : la convergence hémisphérique (PISA) côté aortique, la vena contracta à la sortie de la valve dans la CCVG, et la zone tourbillonnaire allant s’élargissant dans la chambre de chasse et le VG (Vidéo).
Vidéo: Insuffisance aortique sévère en vue long-axe 120°; présence d'une zone d'accélération concentrique en amont; la largeur du jet en aval de la valve représente plus de la moitié de celle de la chambre de chasse.
- Le diamètre de la vena contracta située immédiatement en aval de la valve reproduit la dimension de l’orifice de régurgitation et ne dépend pas de l’hémodynamique ; un diamètre de > 6 mm correspond à une IA sévère.
- Le rapport entre le diamètre de la vena contracta et celui de la CCVG au même endroit est de ≥ 0.6 lors d’une IA sévère. Il se mesure avec le plus de précision en mode TM à travers la CCVG (voir Figure 26.45).
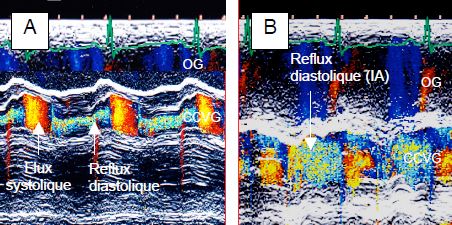
Figure 26.45 : Images en mode TM d’une insuffisance aortique, qui apparaît comme un flux tourbillonnaire holodiastolique. Le rapport entre le diamètre de l’IA et celui de la chambre de chasse est mesurable de manière précise avec cette technique. A : IA modérée; le jet occupe moins du tiers de la CCVG. B : IA severe; le jet occupe presque toute la CCVG.
- PISA: dans les IA modérées, le PISA est faible, aplati et inutilisable pour une quantification. Dans les IA sévères, par contre, il se forme une zone d'accélération concentrique bien visible du côté aortique en diastole qui permet le calcul de la surface de l'orifice de régurgitation comme pour l'IM. Cependant, la valve se présente souvent comme un entonnoir; le résultat doit donc être corrigé pour l'angle formé par la surface non-planaire de la valve (α/180), sans quoi la surface de régurgitation est surestimée: S = (2 π r2 • Valias) / VIA • α/180.
- La planimétrie en 3D évite l'approximation imposée par le 2D qui suppose que l'orifice du flux est circulaire, alors qu'il est typiquement triangulaire, elliptique ou en fente dans l'IA.
Les mesures sont plus fiables dans les IA centrales que dans les IA excentriques. En effet, ces dernières sont liées à une déformation de la valve et peuvent provenir d’un orifice en forme de fente situé à la commissure entre deux cuspides (Vidéo).
Vidéo: Insuffisance aortique centrale s'étendant à la commissure entre la cuspide non-coronarienne et la cuspide coronarienne gauche (vue court-axe 40°).
Leur dimension doit être observée dans plusieurs plans. Dans une maladie aortique, l’axe de l’IA n’est souvent pas le même que l’axe du flux antérograde. Le jet de l'IA apparaît toujours plus important en vue transgastrique (0° ou 120°) car il est situé dans l'axe du faisceau Doppler alors qu'il lui est perpendiculaire dans les vues mi-oesophagiennes. Les mesures de flux sont habituellement exécutées en protodiastole lorsque le gradient transvalvulaire est maximal [21].
Vidéo: Insuffisance aortique centrale s'étendant à la commissure entre la cuspide non-coronarienne et la cuspide coronarienne gauche (vue court-axe 40°).
Leur dimension doit être observée dans plusieurs plans. Dans une maladie aortique, l’axe de l’IA n’est souvent pas le même que l’axe du flux antérograde. Le jet de l'IA apparaît toujours plus important en vue transgastrique (0° ou 120°) car il est situé dans l'axe du faisceau Doppler alors qu'il lui est perpendiculaire dans les vues mi-oesophagiennes. Les mesures de flux sont habituellement exécutées en protodiastole lorsque le gradient transvalvulaire est maximal [21].
Le flux de l’IA enregistré au Doppler continu en vue transgastrique donne une trace spectrale dirigée vers le capteur, dont la silhouette est caractéristique (Figure 11.138) [5,6,9].
- Vélocité maximale : 3-4 m/s. ; la densité de la trace est fonction de l’importance de l’IA.
- Décélération progressive au cours de la diastole ; la pente de cette décélération est directement fonction de la vitesse avec laquelle s’égalisent les pressions entre l’aorte et le VG. Si l’orifice de régurgitation est petit (IA mineure), le ΔP entre l’aorte et le ventricule diminue peu en cours de diastole et la pente est faible. Si l’orifice est grand (IA sévère), le ΔP baisse rapidement au fur et à mesure que le VG se remplit ; la pente est très forte.
- La vélocité télédiastolique permet de mesurer la Ptd du VG ; la Vmax à laquelle le flux cesse en fin de diastole correspond au ΔP entre la pression aortique et la pression intraventriculaire (ΔP = 4 V2IA) ; en soustrayant ce ΔP de la PA diastolique, on obtient la Ptd du VG.
- La pente de décélération de l’IA permet d’en calculer le temps de demi-pression (Pt1/2), qui est le temps nécessaire pour que la pression décroisse de 50% ou la Vmax de 0.7 [6]. Un Pt1/2 de < 250 msec correspond à une IA sévère. La compliance du VG modifie considérablement le Pt1/2: il est raccourci dans une insuffisance diastolique sévère à cause de la pression diastolique élevée du VG et surestime donc l'importance de l'IA [3].
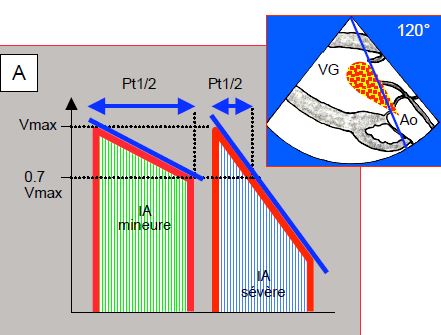

Figure 11.138 : Temps de demi-pression (Pt1/2) de l’insuffisance aortique ; c’est le temps nécessaire à la pression pour diminuer de moitié ou à la Vmax pour diminuer par un facteur de 0.7. L’enregistrement du flux de l’IA se fait dans une vue transgastrique à 0° (vue transgastrique profonde) ou à 120° (vue transgastrique long-axe). A : schéma d’une IA mineure (pente de décélération faible) et d’une IA sévère (pente de décélération forte). B : IA mineure ; Pt1/2 850 msec. C : IA sévère ; Pt1/2 238 msec.
Lorsque l’IA fuit dans le VG, un reflux diastolique apparaît dans l’aorte. Ce flux rétrograde, qui est proportionnel au degré de régurgitation, est visible d’autant plus loin dans l’aorte que la fuite est plus importante [20]. En cas d’IA sévère, il est visible dans l’aorte descendante (Figure 11.139). Sa présence seulement dans l'aorte ascendante n'est pas un critère d'IA sévère.
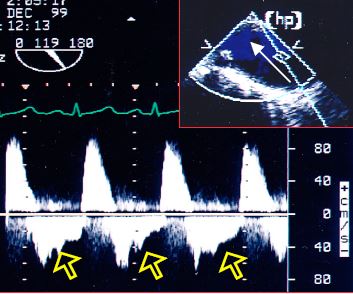
Figure 11.139 : Flux dans l’aorte descendante en cas d’IA sévère, avec présence d’un reflux holodiastolique important (flèches). Le flux est enregistré avec l’axe du Doppler continu le long du bord de l’écran pour être le plus en ligne possible avec le flux dans l’aorte descendante vue en long axe (90-120°).
Les critères échocardiographiques définissant l’IA sévère sont les suivants (voir Tableau 11.13) [9,15,22,25]:
- Hypertrophie dilatative du VG (diamètre télédiastolique > 4 cm/m2) ; absent en cas d’IA aiguë;
- Jet de régurgitation s’étendant jusqu’à mi-ventricule;
- Diamètre de la vena contracta > 0.6 cm;
- Rapport diamètre jet de l’IA/diamètre CCVG > 0.6;
- Pt1/2 du flux diastolique < 250 msec;
- Volume régurgité ≥ 60 ml (fraction de régurgitation ≥ 45%);
- Surface de l’orifice de régurgitation > 0.3 cm2;
- Reflux diastolique dans l’aorte descendante.
Echo 3D
L'image la plus parlante est la reconstruction 3D "en face" de la valve aortique vue depuis l'aorte; la cuspide coronaire droite est l'élément le plus antérieur. Par découpes perpendiculaires à l'axe CCGV-aorte, on peut mesurer le diamètre et la surface de section de la CCVG et de l'anneau aortique, qui sont elliptiques et non circulaires, alors que l'écho 2D n'a accès qu'à la mesure du petit diamètre [21]. La planimétrie de l'ouverture valvulaire en systole et en diastole est réalisable dans 92% des cas [11].
Il est recommandé de procéder en plusieurs étapes pour l’imagerie 3D (Figure 11.140) [14,16].
- Centrer l’image de la valve en court-axe et en long-axe au milieu de l’écran ; la qualité de l’image 2D détermine celle de la reconstruction 3D.
- Acquisition en mode full volume d’un volume contenant la CCVG, la racine aortique et le début de l’aorte ascendante; l’enregistrement se fait en apnée.
- Orientation des plans transverse, sagittal et coronal sur le volume reconstruit.
- Coupe transverse passant par la partie la plus amont des cuspides (points d’articulation avec l’anneau aortique) ; l’anneau est de forme ovale.
- Mesure des diamètres de l’anneau dans le plan sagittal (petit diamètre) et coronal (grand diamètre).
- Mesure de la hauteur des cuspides.
- Mesure des distances entre l’anneau aortique et l’ostium droit (plan sagittal) et entre l’anneau et l’ostium gauche (plan coronal).



Figure 11.140 : Mesures préopératoires de la racine aortique par ETO 3D. A : court-axe de l’anneau aortique (plan transverse). B : long-axe de l’anneau (plan coronal) ; ce plan n’est pas réalisable en ETO 2D. C : mesure de la distance à l’ostium droit. D : mesure de la distance à l’ostium gauche. E: valve aortique normale vue "en-face" en systole et en diastole; la flèche indique la présence d'un cathéter pulmonaire dans l'AP.
Images ETO avant plastie
L'examen ETO avant une plastie aortique doit déterminer le mécanisme de l'IA, l'état des cuspides, la direction du jet de l'insuffisance et la taille de tous les éléments de la racine aortique en fonction de leurs valeurs normales [10,14].
- Diamètres de l'ensemble de la racine aortique en vue long-axe 120-140° ou en reconstruction 3D.
- Anneau aortique: 2.2-2.6 cm;
- Sinus de Valsalva: 3.0-3.4 cm;
- Jonction sino-tubulaire: 2.6-2.9 cm;
- Aorte ascendante proximale: 2.7-3.0 cm.
- Hauteur de coaptation: 5-8 mm;
- Hauteur des cuspides: 1.2-1.4 cm;
- Distance anneau-coronaires: 1.5 cm.
Certains éléments sont à vérifier en fonction du type de lésions [23].
- Type Ia: vérification en télédiastole de la taille de l'anneau aortique et des sinus de Valsalva qui ne doivent pas être dilatés. Le jet d'IA doit être central.
- Type Ib: la jonction sino-tubulaire est effacée et dilatée, dilatation des sinus de Valsalva. L'IA est due à un déplacemnt vers l'extérieur des commissures; l'orifice de régurgitation triangulaire est bien visible en court-axe 40°; l'IA est centrale.
- Type Ic: la dilatation porte sur l'anneau aortique (diamètre > 26 mm); le jet d'IA est central.
- Type Id: le jet couleur est originaire du corps d'une cuspide (perforation, fénestration); sa direction est variable. En court-axe 40°, la commissure est étanche.
- Type II: une cuspide bascule dans la CCVG en diastole et donne un jet d'IA excentrique dirigé vers le côté opposé. Le jet d'un prolapsus de la cuspide coronaire droite est dirigé postérieurement, celui d'un prolapsus de la cuspide coronaire gauche (CG) ou non-coronaire (NC) un jet dirigé antérieurement. La différenciation entre CG et NC n'est pas possible en vue long-axe 120-140° mais seulement en vue court-axe 40° ou en 3D. Le prolapsus peut constituer une simple bascule de l'extrémité distale d'une cuspide ou être complètement éversé dans la CCVG (flail leaflet); dans ce deuxième cas, la coupe en court-axe de la CCVG montre une structure circulaire qui est la section de la cupule prolabante.
- Type III: les feuillets sont fibrosés, rétractés, partiellement calcifiés et les commissures fusionnées en court-axe 40°. En systole, on voit en général une déformation en dôme comme dans la bicuspidie (voir Figure 11.150C). Le jet de l'IA est plus ou moins central selon le degré de symétrie des lésions.

Figure 11.150 C: Image ETO en long axe d'une valve aortique insuffisante de type III en systole. Le bord libre des cuspides est trop court pour leur permettre de rejoindre leur position physiologique en systole ; elles sont retenues en position intermédiaire, ce qui donne un aspect en dôme (doming). L'image est analogue à celle d'une bicuspidie.
Contrôle ETO après plastie
Quelques critères simples permettent de se rendre compte très rapidement si la plastie est réussie (Figure 11.141).
- Absence de prolapsus résiduel;
- Coaptation en aval (au-dessus) du plan de l’anneau aortique;
- Hauteur de coaptation > 4 mm;
- Hauteur des cuspides > 8 mm;
- IA résiduelle < mineure.

Figure 11.141: Plastie aortique. Schéma des conditions d’une plastie réussie ; pas de prolapsus, coaptation en aval du plan de l’anneau aortique (1), hauteur de coaptation > 4 mm (2, flèche rouge), hauteur des cuspides > 8 mm (3, flèche bleue), IA résiduelle < mineure (4).
Dès le déclampage de l'aorte et la reprise d'un rythme cardiaque, l'examen de la valve réparée doit rechercher tous les signes avant-coureurs d'un éventuel échec de la plastie [12,23].
- Le niveau de base de la coaptation des cuspides doit être situé au-dessus (en aval) du plan de l'anneau; une coaptation située au niveau de l'anneau ou en-dessous dans la CCVG est directement lié à une récidive de l'IA. Même en l'absence de fuite diastolique, la coaptation dans la CCVG est un critère de reprise immédiate.
- La hauteur de la coaptation doit être d'au moins 6-8 mm; l'extrémité des cuspides en systole doit se situer à mi-hauteur des sinus de Valsalva (distance avec l'anneau aortique d'au moins 10 mm). Une hauteur de coaptation < 4 mm et une distance entre l'anneau aortique et l'extrémité distale de la coaptation < 6 mm sont directement associées aux récidives d'IA.
- Doppler couleur: tout jet d'IA correspondant à une insuffisance plus que triviale ou mineure (degré > 1) signe un échec de la plastie.
- Gradient systolique transaortique < 10 mmHg; un gradient maximal et un gradient moyen supérieurs à 30 et 15 mmHg, respectivement, sont inacceptables. Un état de haut débit passager et une contre-pulsion intra-aortique peuvent surestimer significativement le gradient.
- Prédicteurs majeurs d'échec: IA résiduelle (OR 5.3), coaptation en-dessous du plan de l'anneau (OR 7.9), hauteur de coaptation < 4 mm (OR 9.1) [8,12].
- La différenciation entre IA mineure et IA modérée est cruciale, car elle signifie l'acceptation du résultat dans le premier cas mais le retour en pompe dans le second [21].
Certains points précis sont à rechercher en fonction du type d'intervention selon la catégorie d'IA (voir CEC et post-CEC pour les illustrations des différentes opérations) [23].
- Type Ia: prothèse tubulaire rétablissant la taille normale de la jonction sino-tubulaire et resuspendant les commissures. Une IA résiduelle peut être due à un prolapsus non détecté avant l'opération ou à un sous-dimensionnement de la prothèse.
- Type Ib: remplacement de la racine aortique par une prothèse de Bentall ou remodelage/réimplantation préservant la valve (opérations de Yacoub et de Tirone David). A l'ETO, on peut suivre la prothèse jusqu'au niveau de l'anneau (double strie); les sinus de Valsalva apparaissent en général plus larges. L'examen de la cinétique segmentaire ventriculaire permet de s'assurer que les réimplantations coronariennes sont bien perméables; le Doppler couleur y montre un flux proximal systolo-diastolique.
- Type Ic: l'annuloplastie à la jonction ventriculo-aortique doit assurer une coaptation normale des feuillets.
- Type Id: le patch de fermeture rigidifie la cuspide et peut gêner la coaptation.
- Type II: l'opération consiste en plicature, résection triangulaire, resuspension, implantation de patch et souvent annuloplastie sous-commissurale. La cuspide concernée apparaît épaissie et moins mobile; les pledgets de la commissuroplastie se manifestent comme une structure dense avec un cône d'ombre. Les gradients permettent de vérifier que la commissurotomie n'est pas trop restrictive.
- Type III: ces lésions conduisent plus souvent à un remplacement par une prothèse et qu'à une plastie (commissurotomie, pelage des cuspides, décalcification, extension par du péricarde).
Fonction du VG
Jusqu'à la phase de décompensation, la précharge reste haute et la postcharge s’élève ; la fraction d'éjection (FE) tend à surestimer la fonction réelle du VG, et ne traduit pas la baisse progressive de sa contractilité. Dans ces conditions, une valeur de 0.5 signe déjà une atteinte significative. Comme c'est le cas pour l'insuffisance mitrale, les dimensions télésystoliques sont un meilleur critère de la fonction du VG ; la fonction est altérée lorsque le Dts est > 4 cm ou > 2.5 cm/m2, et le volume télésystolique (Vts) > 50 mL/m2. La souplesse de la paroi est assez bien conservée, mais la courbe de compliance diastolique est redressée à cause de la tension excessive exercée sur cette paroi.
L’écho permet également de calculer des indices de contractilité qui dépendent moins des conditions de charge et de fréquence, comme la vélocité de raccourcissement circonférentiel (Vcf) :
Vcf = (Cdiast – Csyst) / Cdiast • Téj
où : C = circonférence
Téj = durée de l’éjection
Autres examens
Une coronarographie n’est pratiquée qu’en présence de symptômes ischémiques, ou au-delà de 45 ans chez les hommes et de 50 ans chez les femmes si un remplacement valvulaire chirurgical est indiqué. Lorsque l’échocardiographie transthoracique et transoesophagienne n’est pas suffisamment performante, le CT-scan multibarrettes offre les images les plus détaillées et les plus précises de la racine aortique grâce à son excellente définition spatiale et à sa capacité à mettre en évidence les lésions calcifiées. L’IRM apporte un maximum de renseignements sur la structure et la fonction du VG, notamment sur la présence de fibrose; elle permet les mesures les plus précises du volume et de la masse du VG mais ne voit pas le calcium.
| Echocardiographie de l’insuffisance aortique |
|
L’échocardiographie permet de définir 3 types d’IA :
- Type I : cuspides normales, dilatation de l’anneau aortique, jet central
- Type II : excès de tissu et de mouvement d’une ou des cuspides, prolapsus, jet excentrique
- Type III : mouvement restrictif des cuspides, calcifications, jet variable
Toujours rechercher soigneusement une IA avant une opération en CEC, car elle peut causer une dilatation aiguë du VG pendant la cardioplégie ou la fibrillation ventriculaire, même si elle est minime.
Signes échocardiographiques :
- Dilatation et sphéricisation du VG, ± dilatation de la racine aortique
- Prolapsus ou restriction des cuspides
- Orifice de régurgitation central triangulaire en court-axe
- Vibration et bombement du feuillet antérieur de la valve mitrale en diastole
- Jet couleur diastolique ± étendu ; Vmax 3-4 m/s
Critère de dysfonction du VG : diamètre télésystolique > 2.5 cm/m2.
Critères échocardiographiques de l’IA sévère :
- HVG dilatative (Dtd VG > 4 cm/m2) ; taille du VG normale en cas d’IA aiguë
- Extension du jet dans le corps du VG (selon conditions hémodynamiques)
- Vena contracta > 0.6 cm, rapport diamètre vena contracta/diamètre CCVG > 0.6
- Surface de l’orifice de régurgitation > 0.3 cm2
- Pt1/2 flux diastolique < 250 msec
- Volume régurgité ≥ 60 mL, fraction de régurgitation > 45%
- Reflux diastolique dans l’aorte descendante
|
© CHASSOT PG, BETTEX D, Août 2011, dernière mise à jour Août 2018
Références
- BAUMGARTNER H, FALK V, BAX JJ, et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J 2017; 38:2739-86
- BOODHWANI MJ, DE KERCHOVE L, GLINEUR D, et al. Repair-oriented classification of aortic insufficiency: impact on surgical techniques and clinical outcomes. J Thorac Cardiovasc Surg 2009; 137:286-94
- CHERRY SV, JAIN P, RODRIGUEZ-BLANCO YF, FABBRO M. Noninvasive evaluation of native valvular regurgitation: a review of the 2017 American Society of Echocardiography Guidelines for the perioperative echocardiographer. J Cardiothorac Vasc Anesth 2018; 32:811-22
- EL KHOURY G, GLINEUR D, RUBAY J, et al. Functional classification of aortic root/valve abnormalities and their correlation with etiologies and surgical procedures. Cur Opin Cardiol 2005; 20:115-21
- GRAYBURN PA, HANDSHOE R, SMITH MD, et al. Quantitative assessment of the hemodynamic consequences of aortic regurgitation by means of continuous wave Doppler recordings. J Am Coll Cardiol 1987; 10:135-41
- GRAYBURN PA, HANDSHOE R, SMITH MD, et al. Quantitative assessment of the hemodynamic consequences of aortic regurgitation by means of continuous wave Doppler recordings. J Am Coll Cardiol 1987; 10:135-41
- HYATSVILLE M. Monthly vital statistics reports. National Center for Health Statistics. Report of final mortality statistics 1999; 47(19)
- KARI FA, SIEPE M, HAN-HINRICH S, et al. Repair of the regurgitant bicuspid and tricuspid aortic valve: background, principles, and outcomes. Circulation 2013; 128:854-63
- LANCELLOTTI P, TRIBOUILLOY C, HAGENDORFF A, et al. Recommendations for the echocardiographic assessment of native valvular regurugitation: an executive summary from the EACI. Eur Heart J Cardiovasc Imaging 2013; 14:611-44
- LANG RM, BADANO LP, MOR-AVI V, et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. J Am Soc Echocardiogr 2015; 28:1-39
- LANG RM, BADANO LP, TSANG W, et al. EAE/ASE recommendations for image acquisition and display using three-dimensional echocardiography. Eur Heart J Cardiovasc Imaging 2012; 13:1-46
- LE POLAIN DE WAROUX JB, POULEUR AC, ROBERT A, et al. Mechanisms of recurrent aortic regurgitation after aortic valve repair. Predictive value of transesophageal echocardiography. JACC Cardiovasc Imaging 2009; 2:931-9
- MICHELENA HI, ABEL MD, SURI RM, et al. Intraoperative echocardiography in valvular heart disease: An evidence-based appraisal. Mayo Clin Proc 2010; 85:646-55
- MUKHERJEE C, HEIN F, HOLZHEY D, et al. Is real-time 3D transesophageal echocardiography a feasible approach to detect coronary ostium during transapical aortic valve implantation? J Cardiothorac Vasc Anesth 2013; 27:654-9
- NISHIMURA RA, OTTO CM, BONOW RO, et al. 2014 AHA/ACC Guideline for the management of patients with valvular heart disease. Circulation 2014; 129:e521-e643
- PATEL PA, FASSL J, THOMPSON A; et al. Transcatheter aortic valve replacement – Part 3: the central role of perioperative transesophageal echocardiography. J Cardiothorac Vasc Anesth 2012; 26:698-710
- PATEL PA, GUTSCHE JT, VERNICK WJ, et al. The functional aortic annulus in the 3D era: focus on transcatheter aortic valve replacement for the perioperative echocardiographer. J Cardiothorac Vasc Anesth 2015; 29:240-5
- PERRY GJ, HELMCKE F, NANDA NC, et al. Evaluation of aortic insufficiency by Doppler color flow mapping. J Am Coll Cardiol 1987; 9:952-9
- PRODROMO J, D'ANCONNA G, AMADUCCI A, et al. Aortic valve repair fort aortic insufficiency: a review. J Cardiothorac Vasc Anesth 2012; 26:923-32
- SUTTON DC, KLUGER R, AHMED SU, et al. Flow reversal in the descending aorta: a guide to intraoperative assessment of aortic regurgitation with transesophageal echocardiography.J Thorac Cardiovasc Surg 1994; 108:576-82
- SZYMANSKI T, MASLOW A, MAHMOOD F, et al. Three-dimensional imaging of the repaired aortic valve. J Cardiothorac Vasc Anesth 2016; 30:1599-610
- VAHANIAN A, ALFIERI O, ANDREOTTI F, et al. Guidelines on the management of valvular heart disease (version 2012). The Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2012; 33:2451-96
- VAN DYCK MJ, WATREMEZ C, BOODHWANI M, et al. Transesophageal echocardiography evaluation during aortic valve repair surgery. Anesth Analg 2010; 111:59-70
- ZAMORANO JL, BADANO LP, BRUCE C, et al. EAE/ASE recommendations for the use of echocardiography in new transcatheter interventions for valvular heart disease. Eur J Echocardiogr 2011; 12:557-84
- ZOGHBI WA, ADAMS D, BONOW RO, et al. Recommendations for noninvasive evaluation of native valvular regurgitation: a report from the ASE developed in collaboration with the SCMR. J Am Soc Echocardiogr 2017; 30:303-71
